Reacciones de precipitación: separando lo soluble de lo insoluble

¿Qué son las reacciones de precipitación? La reacción de precipitación es la reacción que ocurre entre dos sustancias en un medio acuoso, donde se forma un producto que no se disuelve en el agua. Esta reacción se puede identificar fácilmente por la formación de un sólido que precipita, por eso, a este sólido también se le llama precipitado.
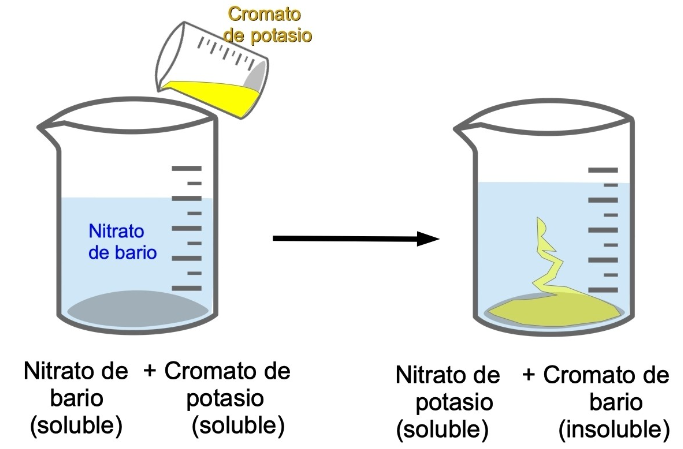
Por lo general, las reacciones de precipitación se producen con compuestos iónicos, es decir, compuestos que en agua se separan en sus iones constituyentes. Por ejemplo, el cromato de potasio se separa en ion cromato CrO2-4 e ion potasio, mientras el nitrato de bario se separa en ion nitrato e ion bario.
Reglas de formación de precipitados
Para reconocer una reacción de precipitación, debemos predecir si el producto que se forma es soluble o insoluble en agua. Para esto, existen las siguientes reglas:
- El compuesto sólido debe tener carga igual a cero. Por eso, dos aniones o iones con carga negativa no pueden combinarse, así como tampoco dos cationes o iones con carga positiva.
- Para que el compuesto no tenga carga, debe combinarse un catión y un anión que compensen sus cargas entre sí.
- La mayoría de las sales de nitrato son solubles.
- La mayoría de las sales que contienen iones metales alcalinos y el ión amonio son solubles.
- La mayoría de las sales con cloro, bromo o yodo son solubles, excepto cuando están presentes los iones plata, plomo y mercurio.
- La mayoría de las sales de sulfato son solubles, excepto el sulfato de bario, el sulfato de plomo, el sulfato de mercurio y el sulfato de calcio.
- Los hidróxidos solubles son el hidróxido de sodio y el hidróxido de potasio. Los compuestos medianamente solubles son el hidróxido de bario, hidróxido de estroncio y el hidróxido de calcio.
- La mayoría de los sulfuros, carbonatos , cromatos y fosfatos son ligeramente solubles, con excepción de las sales con los iones de la regla 4.


¡Echémosle un vistazo al siguiente experimento y si puedes pongámonos manos a la obra!




Responses